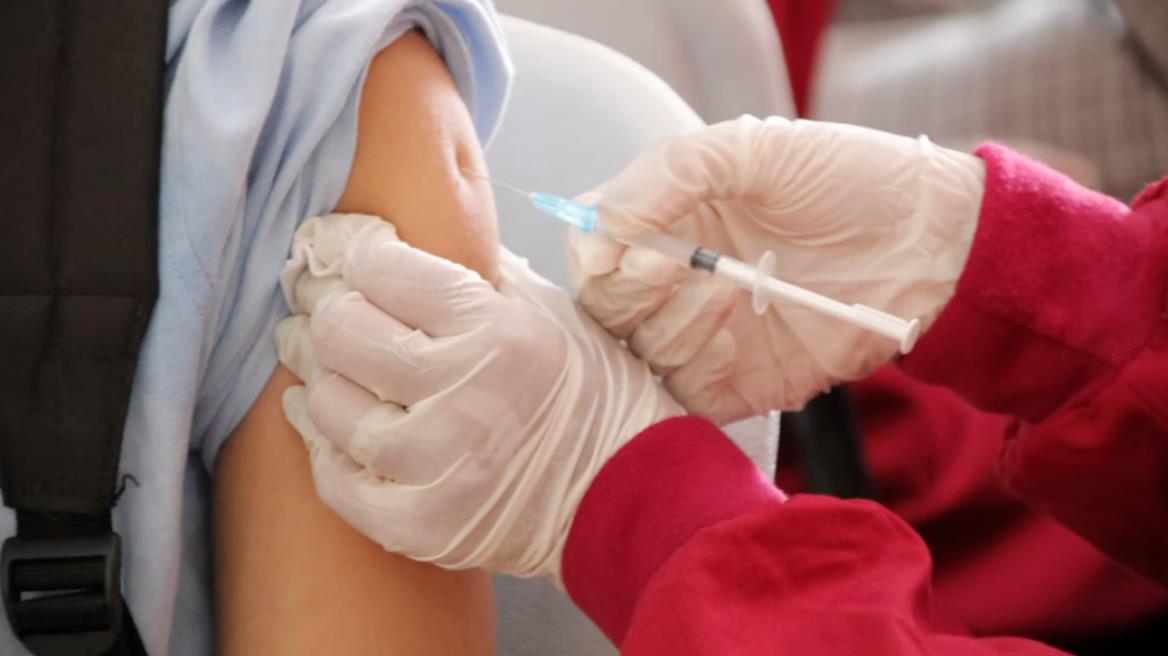
Η Επιτροπή φαρμάκων για ανθρώπινη χρήση (CHMP) του Ευρωπαϊκού Οργανισμού Φαρμάκων (EMA) συνέστησε την αδειοδότηση ενός προσαρμοσμένου εμβολίου Comirnaty που στοχεύει την υποπαραλλαγή Omicron XBB.1.5.
Σύμφωνα με ανακοίνωση του ΕΜΑ, το εμβόλιο – γνωστό ως Comirnaty Omicron XBB.1.5 – πρόκειται να χρησιμοποιηθεί για την πρόληψη της νόσου COVID-19 σε ενήλικες και παιδιά ηλικίας από 6 μηνών και άνω.
Σύμφωνα με προηγούμενες συστάσεις του EMA και του Ευρωπαϊκού Κέντρου Πρόληψης και Ελέγχου Νοσημάτων (ECDC), οι ενήλικες και τα παιδιά ηλικίας από 5 ετών που χρειάζονται εμβολιασμό θα πρέπει να κάνουν μία δόση, ανεξάρτητα από το ιστορικό εμβολιασμού τους έναντι της νόσου COVID-19.
Τα παιδιά ηλικίας από 6 μηνών έως 4 ετών δύνανται να λάβουν μια ή τρεις δόσεις ανάλογα με το εάν έχουν ολοκληρώσει το αρχικό σχήμα εμβολιασμού ή έχουν νοσήσει από τη νόσο COVID-19.
Στόχευση Omicron XBB.1.5
Τα εμβόλια έναντι της νόσου COVID-19 προσαρμόζονται έτσι ώστε να ταιριάζουν καλύτερα με τις κυκλοφορούσες παραλλαγές.
Το εν λόγω εμβόλιο αναπτύχθηκε για να στοχεύει την παραλλαγή Omicron XBB σύμφωνα με τις συστάσεις του EMA και του ECDC καθώς και άλλων διεθνών ρυθμιστικών αρχών και του Παγκόσμιου Οργανισμού Υγείας.
Καθώς η υποπαραλλαγή Omicron XBB.1.5 σχετίζεται στενά με άλλες παραλλαγές που κυκλοφορούν αυτήν τη στιγμή, το εμβόλιο αναμένεται να συμβάλει στη διατήρηση της βέλτιστης προστασίας έναντι της νόσου COVID-19 που προκαλείται από αυτές τις άλλες παραλλαγές, καθώς και από την υποπαραλλαγή Omicron XBB.1.5.
Από την αρχική αδειοδότηση του εμβολίου Comirnaty, οι αρχές έχουν αποκτήσει εκτενή γνώση σχετικά με την ασφάλεια του εμβολίου. Οι ανεπιθύμητες ενέργειες είναι συνήθως ήπιες και βραχυπρόθεσμες και περιλαμβάνουν πονοκέφαλο, διάρροια, πόνο στις αρθρώσεις και στους μυς, κόπωση, ρίγος, πυρετό και πόνο ή πρήξιμο στο σημείο της ένεσης. Πιο σοβαρές ανεπιθύμητες ενέργειες ενδέχεται να εμφανιστούν σπάνια.
Ο ΕΜΑ θα προωθήσει τώρα τη σύσταση της CHMP στην Ευρωπαϊκή Επιτροπή για την έκδοση νομικά δεσμευτικής απόφασης σε ευρωπαϊκό επίπεδο.
Όπως και με τα άλλα εμβόλια έναντι της νόσου COVID-19, οι εθνικές αρχές των Κρατών Μελών της ΕΕ θα καθορίσουν τη χρήση αυτού του εμβολίου στα πλαίσια των εθνικών εκστρατειών εμβολιασμού, λαμβάνοντας υπόψη παράγοντες όπως τα ποσοστά λοίμωξης και νοσηλειών, τον κίνδυνο για ευπαθείς ομάδες πληθυσμού και τη διαθεσιμότητα του εμβολίου.
Το Comirnaty εγκρίθηκε για πρώτη φορά στην ΕΕ τον Δεκέμβριο του 2020, με τις προσαρμοσμένες εκδόσεις που στοχεύουν τα στελέχη BA.1 και BA.4-5 να λαμβάνουν αδειοδότηση τον Σεπτέμβριο του 2022.